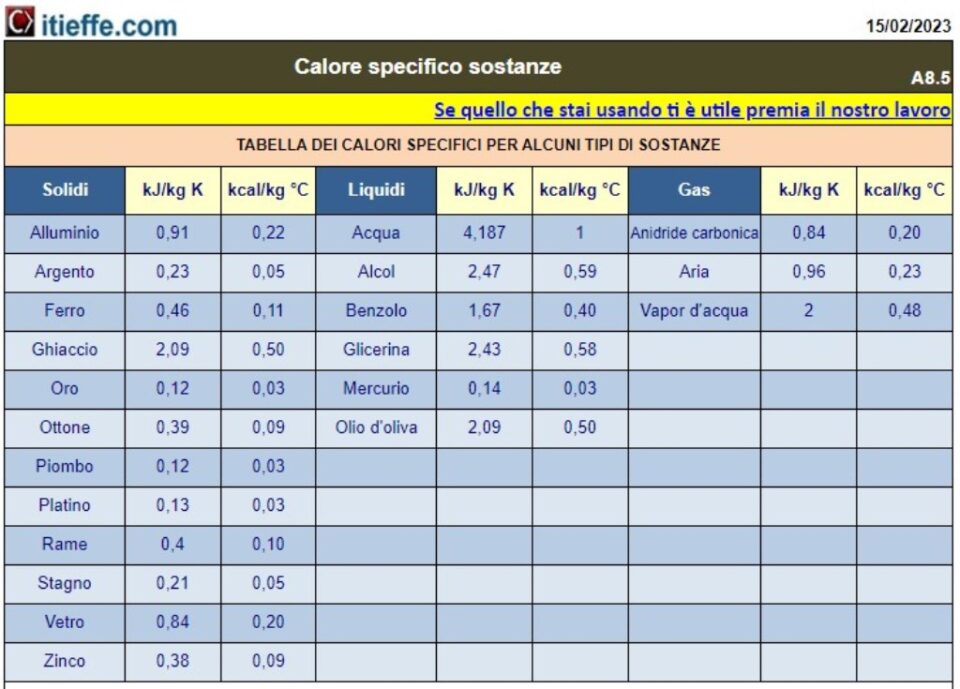
Table thermique spécifique des substances
Cet article créé par Itieffe représente une ressource fondamentale dans le domaine de la thermodynamique et de la science des matériaux, offrant un aperçu détaillé des propriétés thermiques de différentes substances.
Ce document vise à expliquer de manière claire et concise le concept de chaleur spécifique et à fournir des données significatives sur une variété de matériaux, aidant les étudiants, les scientifiques et les ingénieurs à comprendre comment différentes substances réagissent aux changements de température et fournissant des informations essentielles pour la conception de systèmes thermiques et énergétiques. .
Dans cette introduction, nous souhaitons souligner l'importance de la chaleur spécifique comme paramètre fondamental pour la caractérisation thermique des matériaux. La chaleur spécifique représente la quantité d'énergie thermique nécessaire pour élever la température d'une quantité donnée de matière d'un certain nombre de degrés Celsius ou Kelvin.
Cette quantité est cruciale pour un large éventail d’applications, de la conception de moteurs électriques et de circuits de refroidissement au calcul des besoins énergétiques des processus industriels.
Les principales caractéristiques et sujets abordés dans cet article comprennent :
- Définition de la chaleur spécifique : nous expliquerons en détail ce que représente la chaleur spécifique et comment elle est mesurée expérimentalement.
- Unité de mesure: nous illustrerons les unités de mesure de la chaleur spécifique et comment elles sont utilisées dans les formules thermodynamiques.
- Chaleur spécifique de différentes substances : nous fournirons une liste de chaleurs spécifiques pour un large éventail de matériaux courants, notamment les métaux, les liquides, les gaz et autres.
L'objectif principal de cet article est de fournir une image complète du concept de chaleur spécifique et de ses applications pratiques, en aidant les lecteurs à comprendre comment différentes substances réagissent aux changements de température et à faire des choix éclairés dans la conception et l'optimisation des systèmes thermiques et énergétiques. .
La connaissance de la chaleur spécifique des substances est essentielle pour un certain nombre de disciplines scientifiques et techniques, car elle contribue au progrès technologique et à l'efficacité énergétique.
Substances thermiques spécifiques
Substances thermiques spécifiques
La quantité d’énergie qu’un corps chaud transfère à un corps plus froid dépend non seulement de la différence entre les deux températures, mais aussi de la masse du corps le plus chaud. En fait, l’énergie que peut transférer la semelle d’un fer à repasser est bien supérieure à celle que peut transférer une épingle à la même température. La chaleur est donc une quantité étendue de matière. Son unité de mesure est la même que l’énergie, qui en SI est le joule. L’effet provoqué sur un corps par une certaine quantité de chaleur dépend de la nature du corps.
Lorsque, par exemple, nous chauffons 1 kg d’eau et 1 kg de fer avec des quantités de chaleur égales, nous enregistrons des températures finales différentes. Il s’ensuit que, à mesure que la nature du corps varie, la quantité de chaleur nécessaire pour augmenter la température de 1 kg de masse de 1 K diffère. Cette quantité de chaleur est appelée chaleur spécifique.
La chaleur spécifique est la quantité d'énergie absorbée (ou libérée) par 1 kg de matériau qui provoque une augmentation (ou une diminution) de 1 K de la température.
Unités de mesure
L'unité de mesure de la chaleur spécifique, qui est une quantité dérivée, est J/kg K en SI. Les unités J/g K (ou °C) et cal/g °C sont également souvent utilisées, pour l'eau c'est , par exemple, 4186 J/kg K, ce qui correspond à 4,186 J/g °C et 1 cal/g °C
La chaleur spécifique de l'eau est très élevée : c'est-à-dire qu'il faut beaucoup d'énergie pour obtenir de petites augmentations de température. La chaleur spécifique du cuivre, en revanche, est assez faible, de sorte que de petites quantités d'énergie provoquent de fortes augmentations de température. L'instrument qui permet de mesurer la quantité d'énergie transférée est le calorimètre : la quantité d'énergie transférée est le calorimètre : cet appareil enregistre les changements de température que le transfert d'énergie provoque sur un certain corps, généralement de l'eau.
En tenant compte de la masse, de la chaleur spécifique et de la différence de température, l'énergie peut être calculée avec la formule suivante :
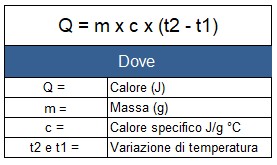
Substances thermiques spécifiques
Le programme ci-dessous est libre d'utilisation.
Pour accéder à la version réservée (voir ci-dessous), pleine page et sans publicité, vous devez être inscrit.
Vous pouvez vous inscrire dès maintenant en cliquant ICI